时间:2022-11-01 22:32
重组腺相关病毒(rAAV)已被广泛用做神经环路研究的示踪工具及基因治疗给药载体,种类繁多的血清型赋予其多样的组织靶向感染特性,究其机制源于AAV衣壳蛋白和细胞表面受体互作的差异,因此,根据实验需求选用恰当的血清型是满足特定外源基因递送需求的重要保证。
在脑实质内原位标记类实验中,向大脑内一些小体积核团递送外源基因,需要局限扩散的AAV载体以避免非目标脑区的感染。在常用于做原位标记的1、2、5、8、9、DJ等血清型中,1型和2型是相对扩散范围较小的血清型,故常被选用于做精准标记,但其仍存在扩散范围较大及原位标记不严谨等问题,因此亟需开发局限原位标记的新型AAV工具。
中科院徐富强团队于2022年10月份发表在《国际分子科学杂志(International Journal of Molecular Sciences)》上题为“AAV13 Enables Precise Targeting of Local Neural Populations”的文章报道了13型AAV具有较常用的2型AAV更小的扩散范围,且未表现出逆行标记或顺向跨突触特性,因此非常适合作为脑实质内精准原位标记工具。

AAV13
表现出更局限的扩散感染
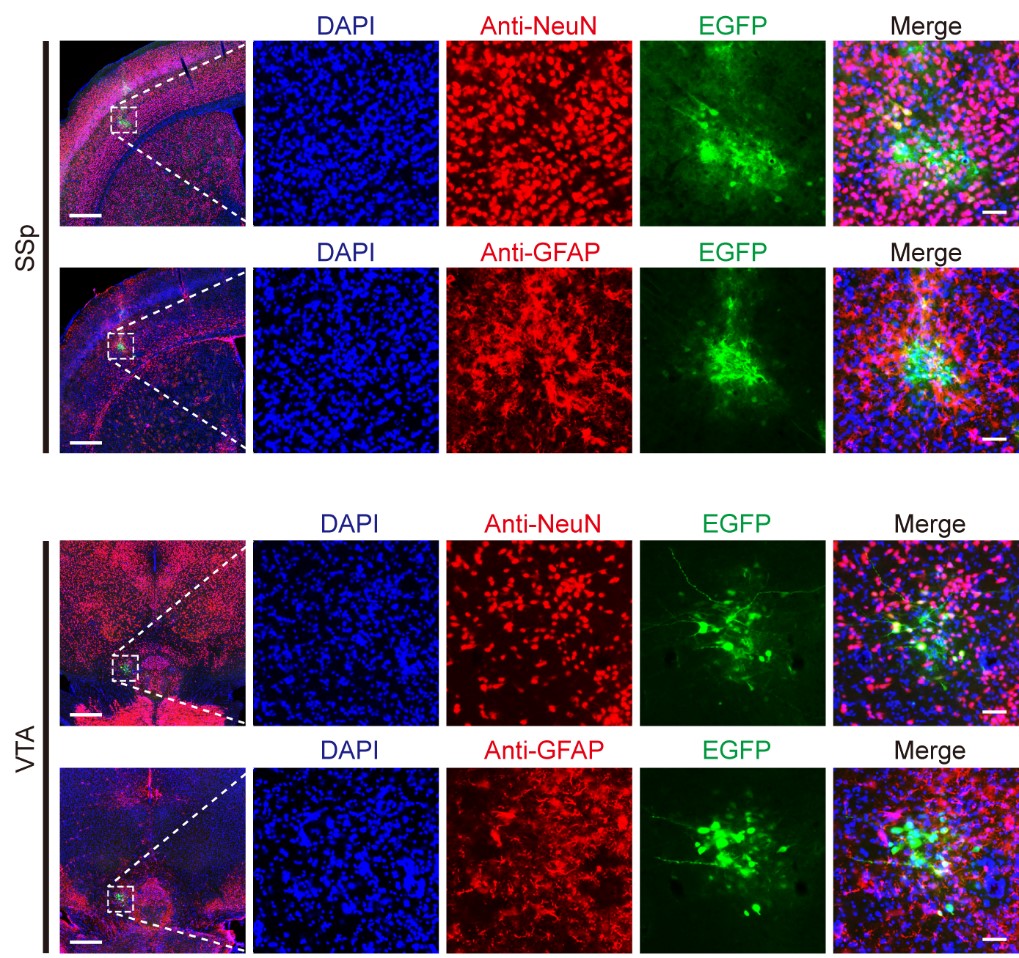
分别在初级感觉皮层(SSp)、中脑腹侧被盖区(VTA)注射AAV13-CMV-EGFP,可见其表现出局限的扩散范围,脑片1/4裁图可见仅有原位感染的一小簇神经元细胞群呈现出绿色荧光。免疫组化显示AAV13主要感染神经元,少量感染星形胶质细胞。
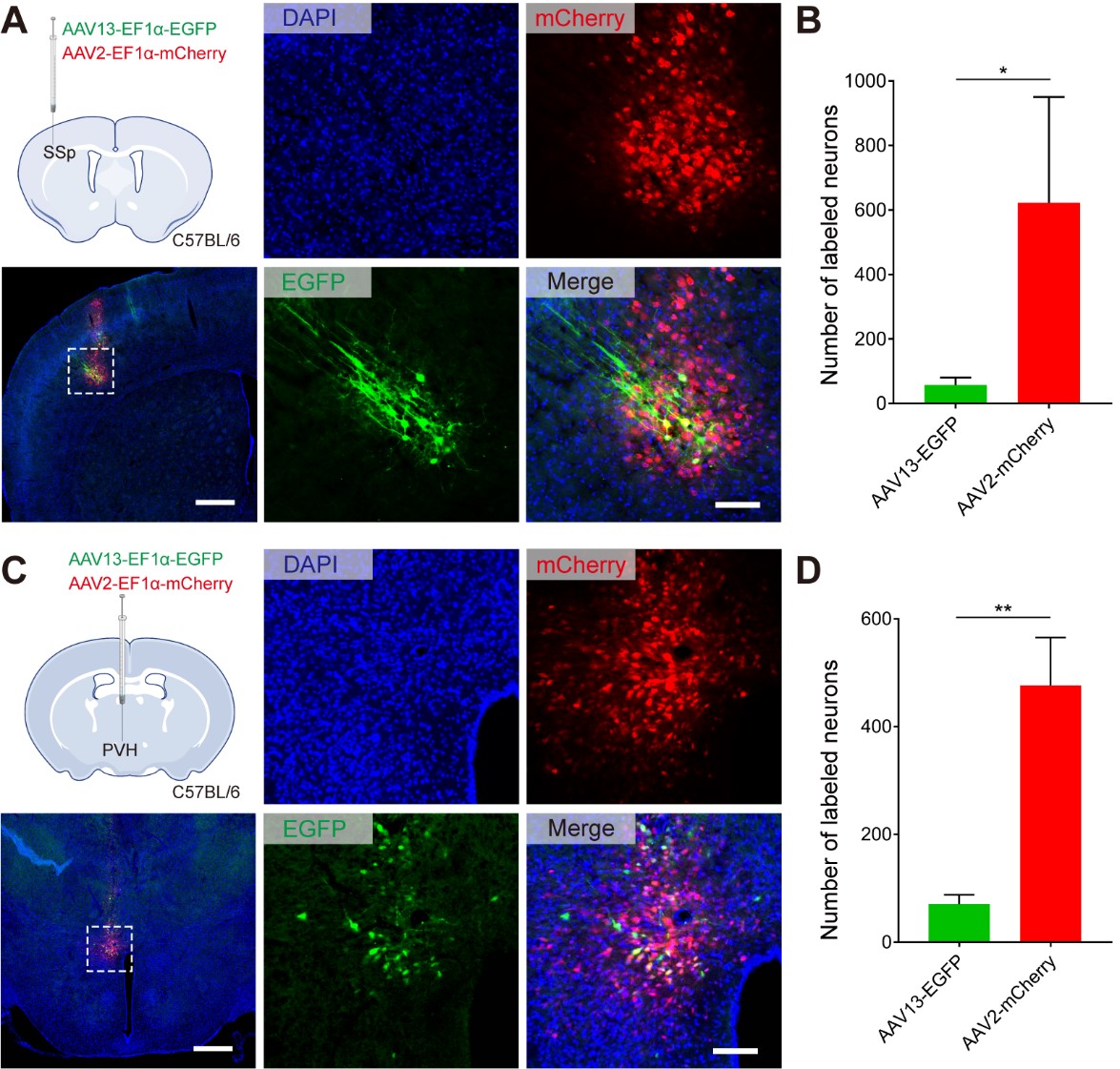
为了评估AAV13原位标记的效果,将AAV13-EGFP与AAV2-mCherry等量混合分别注射在SSp及下丘脑室旁核(PVH,位于下丘脑上部的小体积核团),显示AAV13较AAV2有更小的扩散范围。
AAV13
用于精准稀疏标记
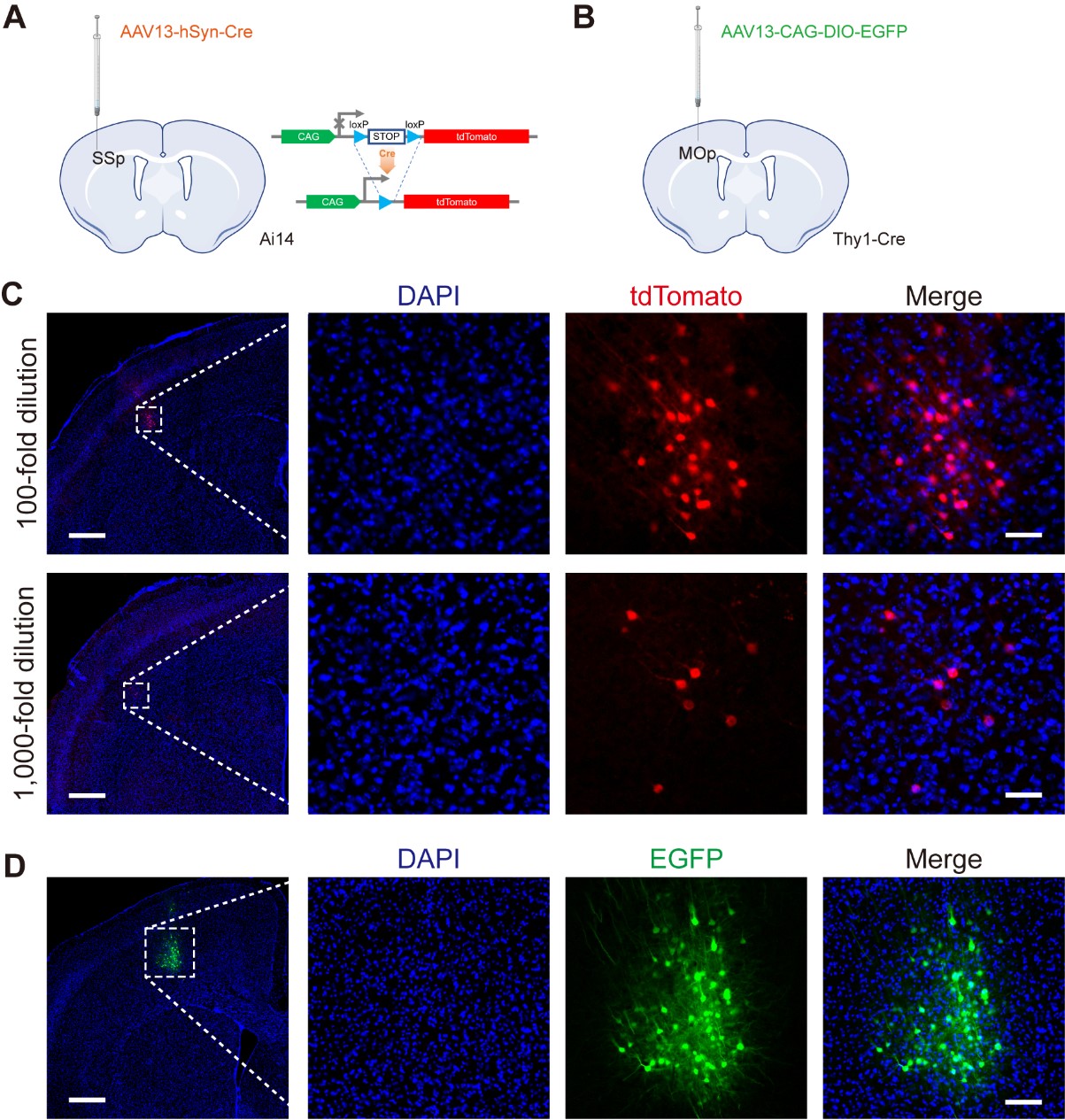
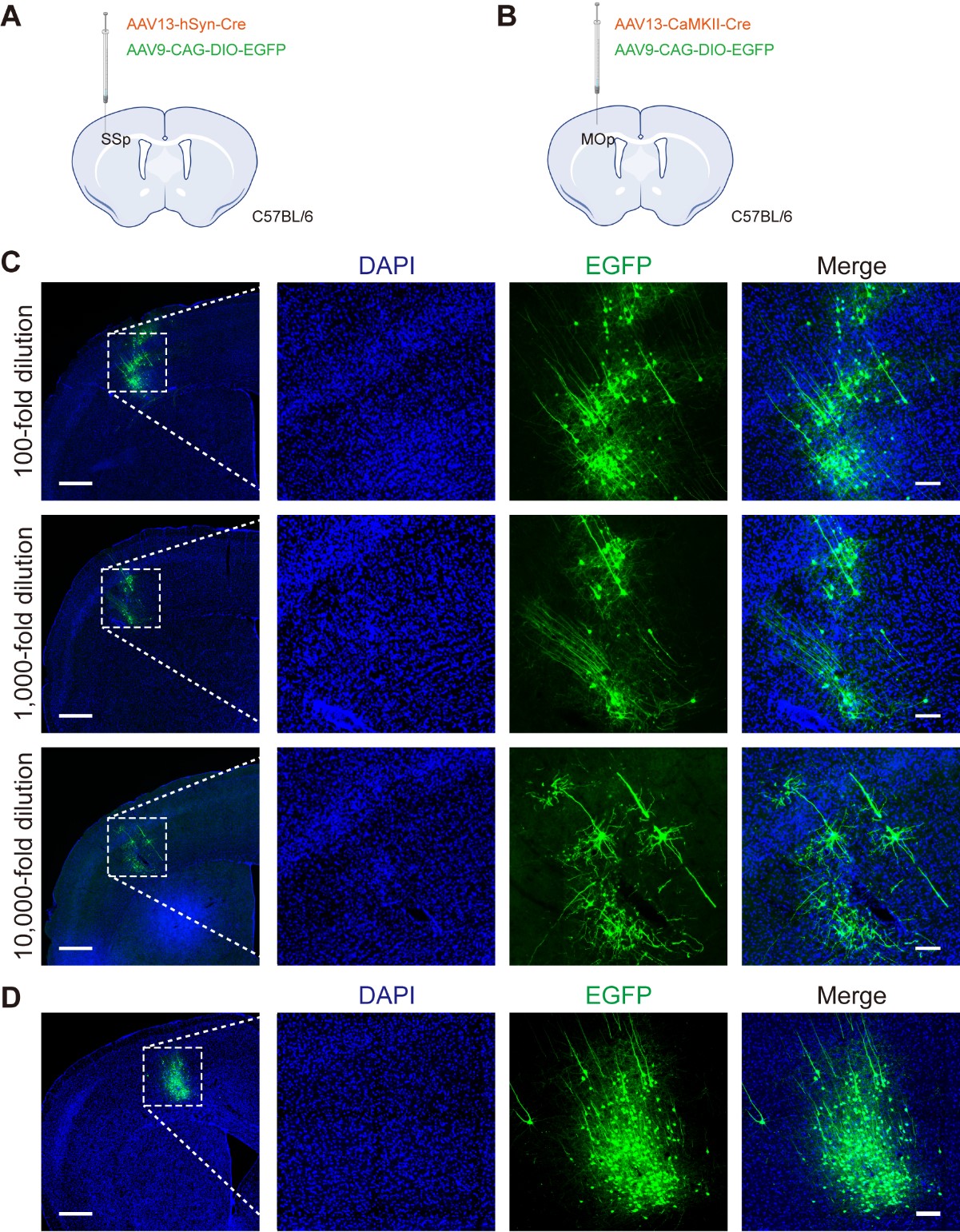
应用AAV13携载Cre重组酶,分别使用单病毒标记策略(AAV13-Cre结合Ai14转基因鼠,或AAV13-CAG-DIO-EGFP结合Cre转基因鼠)或双病毒标记策略(AAV13-Cre和AAV9-CAG-DIO-EGFP)可实现精准位点的稀疏标记。
AAV-Cre作为“控制子”,将报告蛋白的表达锁定在局限的一小簇神经元细胞群,通过稀释滴度控制感染神经元的稀疏度,从而实现“精准稀疏”,配合AAV9-DIO-EGFP等“放大子”的高强度荧光表达,从而实现“高亮标记”。
AAV13
用于功能监测
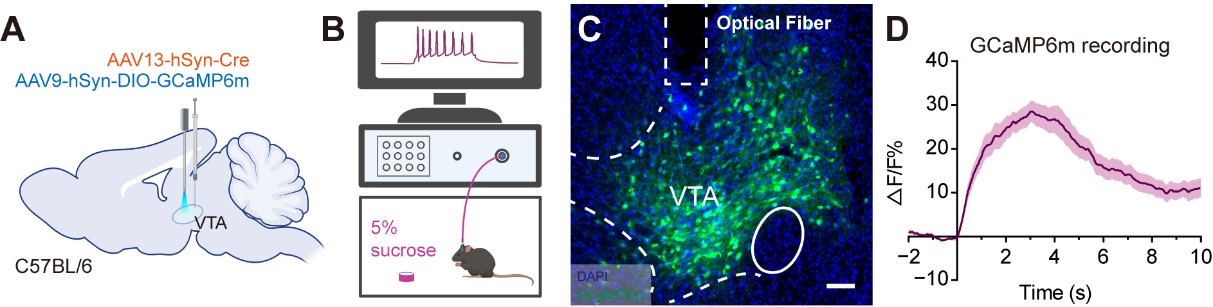
除用于结构网络标记外,AAV13携载Cre元件,也可实现神经元功能监测。AAV13-Cre与Cre诱导载体AAV9-DIO-GCaMP6m注射在VTA,与预期一样VTA神经元被标记,并在小鼠舔糖水时记录到钙信号增加。
AAV13
总结
这些研究工作证实了局限扩散的AAV13可作为新型原位标记载体用于精准原位标记,相较于其它原位标记载体,AAV13直接携载报告基因也存在表达强度弱等问题,进一步的优化工作已在进行中,目前AAV13通过携载Cre酶作为“控制子”限定感染范围是更优的选择。
唐诗有云:“月黑见渔灯,孤光一点萤”,AAV13在大脑内的标记效果正如在茫茫神经元集群里点亮一小团萤火。
以“解密大脑黑匣子”为己任的香港宝典免费资料网,也冀望给在未知海洋里觅航路的科研工作者点一盏“渔灯”,微微风簇浪,散作满河星。
原文链接:
https://www.mdpi.com/1422-0067/23/21/12806
