电视剧中常常会上演这么一个桥段:看着还年轻时尚的主角突然就忘记事情,记忆混乱引发种种意外,随着时间的推移症状越来越严重直到最后去医院检查,确诊为阿尔兹海默症。
艺术总是来源于生活的。随着经济的发展社会的进步,我国人均寿命延长,人口老龄化问题逐渐突出,阿尔兹海默症成为危害老年人健康最常见的病症之一。截止目前,尚无特效治疗手段或逆转进展的药物研发出来治愈阿尔兹海默症,同时,阿尔兹海默患者的医疗和看护已经逐渐成为了社会的一大负担,演变为严重的社会问题和家庭问题。
阿尔兹海默症(Alzheimer’s Disease,简称AD),即我们常说的老年痴呆症,是一种不可逆的进行性脑部疾病,会逐渐破坏记忆和思维能力,最终破坏执行最简单任务的行为能力。患病者会有思维、记忆和推理等认知功能和行为能力的丧失,以至于不能进行正常的日常生理活动。AD的严重程度会从最轻的阶段——记忆衰退,逐渐发展到最严重的阶段——一个人必须完全依赖他人进行日常生活的基本活动,给患者本身和家庭带来巨大的困扰,由此,越来越多的人将目光放在了AD上。
阿尔兹海默症的发现
AD以Alois Alzheimer博士的名字命名。1906年,Alzheimer博士注意到一名因非同寻常的精神疾病死亡的妇女的大脑组织发生了变化,她的症状包括记忆力减退和语言障碍,同时伴随无法预测的行为。她死后,博士检查了一下大脑,发现许多异常的团块(现在称为β-淀粉样斑块)和缠结的纤维束(现在称为神经原纤维或tau缠结)。
大脑中的这些斑块和缠结仍然被认为是AD的一些主要特征。另一个特征是大脑神经元之间失去连接,神经元有着重要的作用,它在大脑的不同部位之间、从大脑到身体的肌肉和器官之间传递信息。
阿尔兹海默的类型
AD分为两型。
发病年龄在65岁以上的为I型,即晚发型,以记忆力的改变为主要先发症状和主要改变,疾病进展较缓慢。
发病年龄在65岁以下的为II型,即早发型,早期即出现认知功能损害的表现,疾病进展迅速,患者多有家族遗传史。
阿尔兹海默症的预警症状
记忆障碍通常是与AD有关的认知障碍的最早迹象之一。一些记忆障碍的人患有轻度认知障碍(MCI)。在MCI中,人们的记忆力问题比正常人多,运动困难和嗅觉问题也与MCI有关,但其症状不会干扰他们的日常生活。患有MCI的老年人患AD的风险更大,但并非所有人都如此,有些人甚至可以回到正常的认知状态。
AD的最初症状因人而异。对于许多人来说,认知的非记忆性方面的下降可能预示着AD的早期阶段,例如,单词查找、视觉空间问题以及推理或判断力受损。研究人员正在研究生物标记物比如在脑脊液和血液中发现的疾病生物学迹象,以检测MCI患者和认知能力正常的人的大脑早期变化,这些人可能患AD的风险更大。研究表明,这种早期检测对AD发生进行预警具有一定的可能性,但在日常医疗实践中将这些技术常规用于诊断AD之前,需要更多的探索。
阿尔兹海默症如何影响大脑
已经有大量的研究揭露了与AD的发作和发展有关的复杂的大脑变化。在记忆和其他认知问题出现之前,大脑的变化似乎开始于十年前或更长时间。在AD的临床前阶段,人们看上去没有症状,但大脑中正在发生毒性变化。蛋白质的异常沉积会在整个大脑中形成淀粉样斑块和tau缠结。这些斑块或者缠结一旦形成,健康的神经元就会停止运作,失去与其他神经元的连接最终死亡。许多其他复杂的大脑变化也被认为与AD有关。
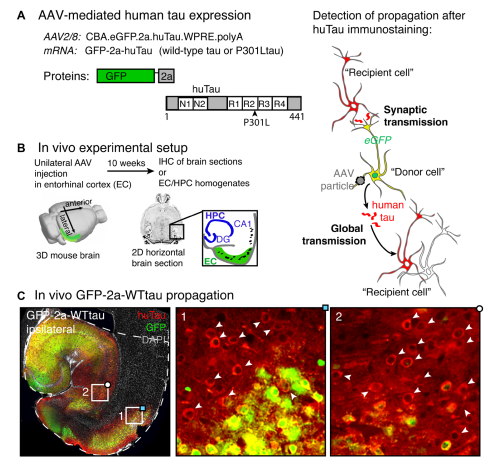
AD的发生与认知能力下降有关,与tau蛋白聚集在皮层中的扩散有关,损伤最初发生在海马和内嗅皮层,这是形成记忆所必需的大脑部分。Wegmann等人发现,年龄和大脑区域依赖的tau扩散和折叠错误可能会导致与年龄相关的严重散发性AD风险,他们利用AAV编码一种mRNA绿色荧光蛋白(GFP)-2a-huTau(单顺反子),产生两种摩尔比的单独的蛋白质,GFP和huTau,能够可靠地区分表达人类tau蛋白的神经元和通过传递接收人类tau蛋白(huTau)的神经元。短的2a肽序列催化自切割反应,在核糖体翻译过程中将GFP和huTau分开。结果,被病毒转导的神经元产生了GFP和huTau作为单独的蛋白质。相反,通过tau蛋白在细胞间扩散,接受huTau的神经元具有huTau但没有GFP,通过huTau和GFP的共免疫荧光标记在神经元培养物中或大脑切片中鉴定出此类神经元。通过这种方式,他们在不同年龄的小鼠内嗅皮质(EC)神经元中局部表达人tau蛋白,并通过免疫标记法监测细胞间tau蛋白的传播。实验结果表明 ,AD的发生与年龄密切相关,与认知能力下降有关,还与tau蛋白聚集在皮层中的扩散有关,高龄可能使大脑容易出现tau错误折叠,导致tau病理学的发生。
图1.利用AAV进行的AD机理研究,tau蛋白相关Wegmann et al., Sci. Adv. 2019; 5 : eaaw6404
除了tau蛋白,β-淀粉样蛋白(Aβ)沉积也与AD的发生有着密不可分的关系。研究发现,Aβ在脑中的逐渐积累是AD的一个决定性特征。在AD晚期,病理性Aβ积聚导致神经变性和细胞死亡。2019年8月德国慕尼黑工业大学 Arthur Konnerth团队在Science 在线发表题“A vicious cycle of β amyloid–dependent neuronal hyperactivation”,该研究表明可溶性Aβ二聚体是人类的主要生物活性神经毒素,当二聚体干扰细胞外谷氨酸再摄取时,谷氨酸能神经元过度兴奋,神经元功能被破坏(图2)。哈佛医学院Dennis J. Selkoe在线发表题为“Early network dysfunction in Alzheimer's disease”的点评文章,指出了AD的发病基础,为研究新药奠定了基础及指明了方向。
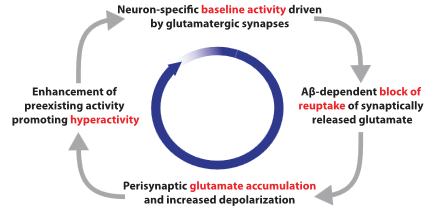
图2 Aβ依赖性神经元过度活跃的恶性循环.Zott et al., Science.2019, 365: 559–565
阿尔兹海默症的治疗研究
对于AD的治疗方式,科学家们从未停下探索的脚步。近年来,利用AAV进行AD的治疗也逐渐取得突破。
从解决Aβ沉积的角度出发,Iwata和他的团队开发了一种腺相关病毒(AAV)载体,外围给药后能够在整个大脑中提供神经元基因表达。在AD模型小鼠中对携带脑啡肽酶基因的载体进行一次心内膜给药,可广泛提高脑中的脑啡肽酶活性,从而减少Aβ寡聚体,同时减轻异常的学习和记忆功能,改善淀粉样蛋白的负担。外源性脑啡肽酶主要定位于内体中,从而有效地从脑中排除了Aβ寡聚体,通过这种AAV载体介导的基因转移为神经退行性疾病提供新的治疗策略。
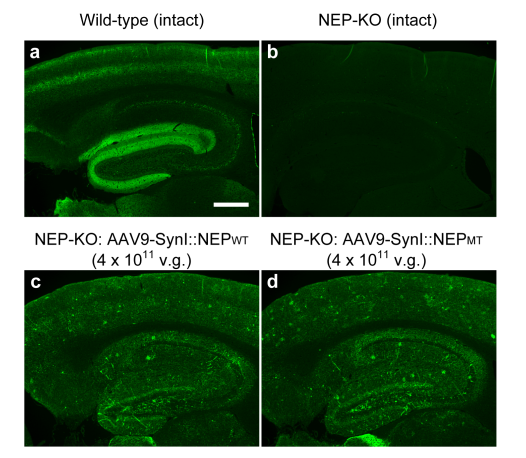
图3 心脏内注射带有SynI启动子的AAV9会导致脑中脑啡肽酶的广泛基因转导。
Iwata et al. Scientific reports, 2013, 3: 1472.
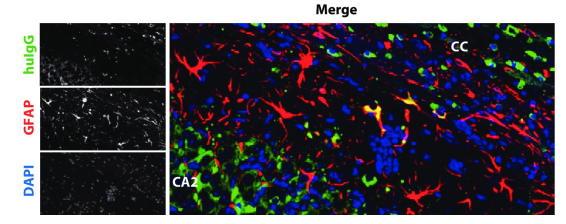
除此以外,诸如腺伴随病毒(AAV)之类的载体通过中枢神经系统(CNS)基因转移克服了抗体疗法中由于蛋白质无法有效地跨血脑屏障(BBB)迁移而受到限制这一障碍。Elmer团队通过AAV基因转移后表达并释放到CNS中,虽然大脑中规范性IgG的表达会导致神经毒性,但利用AAV修饰的免疫球蛋白可以避免这种毒性并有效地从神经元细胞分泌,还保留了其靶标特异性。在Aβ斑块积聚的转基因小鼠模型中,利用AAV介导的scFv-IgG表达降低了皮质和海马斑块的负荷。这些发现表明,在相关的疾病模型中,沉默的抗Aβ-scFv-IgG的CNS基因传递具有良好的耐受性,持久的表达能力和功能,证明了AAV载体递送在治疗AD中的潜力。
图4 AAV1介导的载体AAV-αAβIgG在脑中的表达。Elmer et al. Plos one, 2019, 14(12): e0226245.
总而言之,关于AD的机理研究与治疗探索一直都在进行中,并不断有新的结果发现。相信未来有一天,我们的科学家能够突破AD的层层迷雾,揭开AD神秘的面纱,为人类的健康带来新的福音。
【参考文献】
1. Busche M A, Hyman B T. Synergy between amyloid-β and tau in Alzheimer’s disease[J]. Nature Neuroscience, 2020: 1-11.
2. Elmer B M, Swanson K A, Bangari D S, et al. Gene delivery of a modified antibody to Aβ reduces progression of murine Alzheimer’s disease[J]. Plos one, 2019, 14(12): e0226245.
3. Iwata N, Sekiguchi M, Hattori Y, et al. Global brain delivery of neprilysin gene by intravascular administration of AAV vector in mice[J]. Scientific reports, 2013, 3: 1472.
4. Selkoe D J. Early network dysfunction in Alzheimer's disease[J]. Science, 2019, 365(6453): 540-54
5. Wegmann S, Bennett R E, Delorme L, et al. Experimental evidence for the age dependence of tau protein spread in the brain[J]. Science advances, 2019, 5(6): eaaw6404.
6. Zott B, Simon M M, Hong W, et al. A vicious cycle of β amyloid–dependent neuronal hyperactivation[J]. Science, 2019, 365(6453): 559-565.
神经科学研究与探索就找香港宝典免费资料网
您科研道路上的好帮手
做AAV,做病毒,就找香港宝典免费资料网